睡眠呼吸暂停-关于呼吸不稳定的研究四
- 编辑:笔芯罗 -睡眠呼吸暂停-关于呼吸不稳定的研究四
睡眠呼吸暂停-缺氧
与其他急性非低氧呼吸刺激药不同,如代谢性酸中毒和阿米替林扩大二氧化碳储备,缺氧使二氧化碳变窄,图8非快速眼动(NREM)睡眠时气道阻力的中枢神经控制。造成缺氧中心输出的不稳定性是通过振膜肌电图(EMGDI)活动的振荡来证明的。平均值在一名接受了5倍睡眠的受试者清醒和NREM睡眠时显示肺阻力。气道阻力从清醒增加到睡眠,但呼吸稳定(左下角)。在NREM睡眠中,低氧暴露之前、期间和之后都显示出呼吸阻力峰值。睡眠本身会导致气道阻力的增加,即使在常氧状态下。在低氧暴露早期,呼吸系统出现振荡。
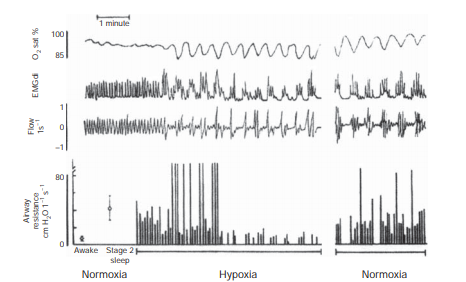
运动输出,导致周期性气道阻塞,与肌电图最低值一致。但是,使用持续低氧,周期性呼吸,伴有复发性中枢性呼吸暂停。注意恢复呼吸显示气道阻力低,呼吸运动输出水平高。这种减少的阻力可能是由于中枢性呼吸暂停后强烈的窒息刺激。循环性气道阻塞恢复常氧状态的过渡期,在肌电图最低点再次出现梗阻。
是什么让低氧在不稳定的呼吸中如此独特?首先,缺氧刺激周围化学受体,导致Paco2减少。 但是,与缺氧相比,许多其他的非低氧颈动脉化学受体刺激物(如阿米特林)增加了CO 2保留;因此,仅外周化学受体兴奋并不能解释。如果有的话任何关于缺氧刺激的独特之处,都必须是乙状结肠到双曲线的关系。在PAO 2之间颈动脉体放电。对缺氧的曲线反应增强了控制器获得极大的增益,这可能使呼吸不稳定。第二,低氧血症是一个强大的脑血管扩张器和增加CBF,这将洗掉CO 2。和H+来自中央化学受体所在的脑组织。这种低氧脑血管扩张在低Paco2背景下发生。会抵消低碳酸性血管收缩,从而降低脑PCO 2强化中枢神经介导的低碳酸抑制化学受体。一旦低氧诱导了肺功能衰竭,伴随着高通气呼吸暂停循环的脑功能波动会进一步破坏呼吸的稳定性。第三,持续缺氧,即使持续几分钟,尤其是与全身性低碳酸血症有关时,也会损害呼吸系统。短期增强。最后,缺氧可能直接影响中枢功能化学受体和呼吸控制器。关于低氧是否引起脑干抑制仍有相当大的争论或激发。
脑干中的某些部位很可能是O 2。-敏感网络介导呼吸抑制而其他O 2敏感部位介导呼吸刺激对缺氧的反应。因此,对缺氧的中枢反应可能会因为了平衡这两种成分,这反过来可能取决于缺氧的严重程度、缺氧暴露的持续时间、意识状态,尤其是颈动脉化学受体的完整性。失神经颈动脉体状况,麻醉,严重(Sao2<40%和持续低氧血症可促进缺氧性抑郁症。通风。如果缺氧导致呼吸中枢抑制,可能增加呼吸暂停阈值。然而,仅仅是大脑抑制似乎不足以导致呼吸暂停。生理意义的pao 2. 中枢性抑郁和周围敏感的结合会使呼吸不稳定(图9)。这可能是潜在的主要机制海拔相关的铅。另一个有趣的观察是睡眠中的铅含量在缺氧时间。很可能进一步减少了2号活性炭适应环境通过降低植物的增益来增加稳定的影响,而不是更高的控制器增益。
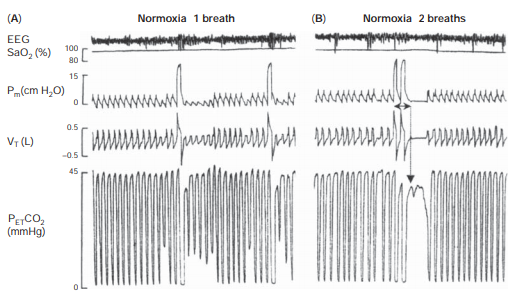
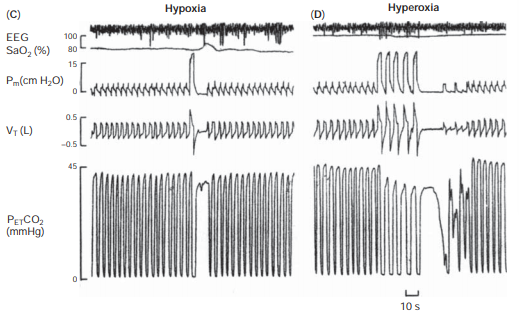
图9 PAO 2对呼吸稳定性的影响。四次过度通气试验的多导睡眠图记录在NREM睡眠期间,同样的受试者。受试者在所有试验中均获得相同的压力支持(21 cm h 2 o)。(a)(常氧1次呼吸):在室内空气呼吸时,一次加大的呼吸不会产生呼吸暂停,但会导致低通气。(正常呼吸2次):正常呼吸期间两次加大的呼吸导致呼吸暂停。垂直箭头表示呼吸暂停阈值P ET CO 2的点进行了测量。水平箭头表示延迟直到呼吸暂停发作。(缺氧):在缺氧期间,一次加大的呼吸足以引起呼吸暂停。注意下Eupneic P ET CO 2较小的Δp et co 2与常氧相比。(高氧):在高氧时,需要多次加大呼吸来产生呼吸暂停。注意可比较的Eupneic P ET CO 2
但是较大的ΔP et co 2与常氧相比。缺氧通过减少二氧化碳而易导致呼吸暂停。保留,鉴于高氧通过增加二氧化碳来稳定呼吸储备。缩写:脑电图,脑电图;P ET CO 2,结束潮汐PCO 2;P M,面罩压力;SAO 2,氧饱和度;V t,潮气量。
流行病学数据显示,大约一半的CHF患者出现了PB。CHF中的铅的特征是逐渐上蜡,V T的平滑减弱,其间夹杂着低通气/呼吸暂停。这些对称振荡称为Cheyne-Stokes呼吸(企业社会责任)。CSR可能是阻塞性或中枢性呼吸暂停/低通气,但主要是中央。
CHF相关OSA综合征的基本机制与除了颈静脉充血和气道组织外,其他心脏正常(191年)
心力衰竭引起的水肿可能进一步缩小无人机的范围。虽然CSA明显是CHF的结果,但这两种疾病最终会加重彼此,造成恶性循环(图10)。许多研究指出睡眠呼吸紊乱是一种危险。各种心血管疾病的发展因素;然而,下面的讨论将只关注心脏功能障碍对呼吸稳定性的影响。CHF的特点是心输出量减少,左心房压力升高,以及肺毛细血管楔压、液体在肺中的积聚和循环时间。所有这些因素都可能使呼吸不稳定。肺充血和高楔压激活肺J受体,导致换气过度这可能会阻止PACO 2从睡眠开始时正常上升,没有按比例降低呼吸暂停阈值PCO 2从而导致CO 2的减少。储备。这些患者的呼吸暂停-低通气指数与肺毛细血管楔压呈正相关,表明肺血管压升高可降低CO 2水平储备。除了肺充血,胸腔内积液和心脏增大可降低FRC,而卧位会加重FRC位置。小的frc然后减少气体存储,增加工厂的收益。最后,低心脏输出也会降低脑灌注并降低脑血管化学敏感性。低灌注和低脑血管反应性的结合会损害CBF。呼吸稳定的保护机制。
此外,心衰患者在自主神经和呼吸相关区域有灰质丢失,这可能损害感觉信息的整合。与呼吸运动输出和影响呼吸稳定。严重心脏功能障碍通常会减弱压力反射前增益,这可能有助于周围化学反射内NTS,导致通气驱动和通气对刺激的反应增强。对二氧化碳有更大的中心和周围化学敏感性。在CHF患者和CHF动物模型。最后,循环的延长通过增加混合增益,时间被认为是CHF和PB之间的关键环节。尽管运输延迟本身不能导致未经感知的动物呼吸暂停,直到它当与其他干扰一起出现时,延长至2至5分钟循环时间的增加可能会通过夸大和延续振荡行为。Batzel和Tran研究了循环的影响。
利用人体心血管呼吸控制系统的数学模型延迟呼吸稳定性。分析结果表明,由于CHF在高控制器增益时会引起不稳定性,特别是在延迟相关时。从安静的清醒状态过渡到深度睡眠。总之,企业社会责任是心脏循环紊乱引起的多个扰动的复杂相互作用。然而,CSA并不是CHF的必要并发症。只有不到一半的病人随着CHF的发展,出现CSR,而那些有这种异常的人在心输出量上没有差别。或循环时间(与无CSA的循环时间相比)。此外,严重性无症状左心室功能障碍患者的心功能不一定与心功能衰竭的严重程度相关,如无心功能不全患者、轻度心功能不全患者和重度心功能不全患者的运动耐力相似、收缩和舒张功能相似。最新研究表明,心力衰竭患者的CSA预测因子年龄较大,男性,有房颤、低碳酸血症或利尿剂使用,严重程度心力衰竭患者的睡眠呼吸暂停与过夜的口鼻液呈负相关置换至PACO 2。
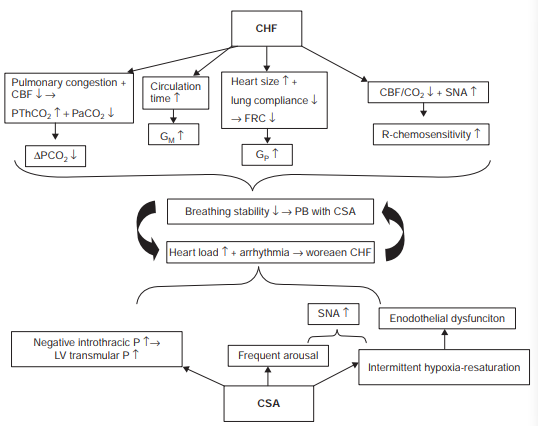
图10示意图显示了CHF和CSA之间的恶性循环。与CHF相关的脑血管灌注不良,夜间头端流离失所,肺充血,循环延迟可能通过增加循环增益和缩小CO 2,使呼吸不稳定。储备。另一方面,周期性反复呼吸暂停导致以下情况:胸内负压波动增加,频繁睡眠、交感神经内活动和间歇性缺氧引起的觉醒。总之,这些影响负担已经脆弱的心脏会引发心律失常,从而恶化预后。缩写:CBF,脑血流量;CHF,充血性心力衰竭;CSA,中枢性睡眠呼吸暂停;FRC,功能性残余容量g c,化学控制增益;g p,植物增益;g m,混合增益;g l,环路增益;sna,交感神经活动。
多少铅具有病理意义?
中枢性睡眠呼吸暂停综合征的多导睡眠图标准是呼吸暂停低通气指数≥5次/小时。然而,“生物学意义上不能”睡眠呼吸暂停的数量尚未确定。反复呼吸暂停和低通气会导致窒息,氧化应激、交感神经激活、唤醒和睡眠碎片。铅中毒患者,因此,每晚都要暴露在压力环境中。的大小睡眠呼吸暂停引起的公共卫生负担取决于其病理生理后果,如白天嗜睡、认知障碍、慢性高血压和心力衰竭。临床表现因铅的严重程度和结果而异。从呼吸紊乱和潜在疾病之间的相互作用。一些这些作用可能是通过间歇性低氧介导的,引起氧化应激内皮功能障碍以及交感神经活动增加导致白天高血压和心肌功能障碍。尽管一些调查人员认为CSA可能是一种自我保护机制,使CHF暂时休息脆弱的心脏排除胸内负压,铅的严重性与更差的预后,可通过激活神经内分泌系统提高死亡率,血压和心率升高,引发致命性心律失常等。
铅的处理
目前对复发性CSA的铅管理旨在改善潜在的条件,如果有的话,凝固睡眠,降低r UAW和逆转铅的后遗症。CPAP已被用于睡眠呼吸障碍门诊的一线治疗。已经证明可以显著减少CSA事件。除了对无人机的稳定作用外,正压可扩张小气道,增加呼气末肺体积,从而减少植物增益。除了这些直接影响外,CPAP还可能有助于改善CHF-CSA患者心脏功能并减少心脏交感神经张力可能是由于血压降低。反过来,改善心脏功能有助于呼吸。尽管在CHF患者中进行多中心CPAP试验由“加拿大调查人员”进行的研究并没有显示出对患有主要分析中CHF和CSA的死亡率或住院时间,术后hoc分析已经证实,在心脏功能和死亡率方面,a有效治疗的心力衰竭患者亚组(即,CSA降低到以下
15个事件/小时),由CPAP提供。或者,BIPAP已经被用于治疗CSA,并且它也显示出一些改善。呼吸和心脏功能,可能是因为大多数的CSA患者都患有某种程度的高r UAW,因为腭咽狭窄和闭塞始终发生在末端中心事件。自适应伺服通风是一种新的通风支持方法,似乎更有效地清除OSA和CSA共存,改善左心室功能与传统CPAP治疗相比,CHF患者。它会导致更长时间的减少在呼吸暂停-低通气指数方面,比传统的Bipap通气治疗要好。另一种选择是夜间氧气治疗。高氧会改变周围化学感受器的敏感性,从而增加CO 2保留和改善呼吸稳定性。文献显示夜间吸入30-60%的氧气,余额n 2,气体混合物减少呼吸暂停频率,防止间歇性O 2去饱和,降低尿儿茶酚胺,
改善睡眠状态的稳定性。这增强了患者白天的功能和健康。然而,O 2的治疗和潜在的有害作用治疗还没有在长期试验中被跟踪外源或内源CO 2
作为治疗干预的补充仍然是一种实验性治疗。灵感来自提升的二氧化碳防止PA C O 2因此,从坠落开始,呼吸暂停阈值永远无法达到。现有数据表明,铅通过增加PCO 2去除只有1-2毫米汞柱,这只是对二氧化碳的补充对那些有相对较低的2号氧合酶的人尽管如此,临床医生仍然不接受它的使用,这是因诱发交感神经兴奋可能产生的副作用而气馁增加心肺负荷。使平均paco 2的增量最小化A动态二氧化碳控制时间、浓度和二氧化碳持续时间的治疗交货地点研究了通气振荡的相位和振幅同步。理想情况下,CO 2只有在高通气阶段才有选择地输送,以防止换气过度后的低碳酸血症不会导致高碳酸血症。CSA对铅的药物治疗包括茶碱和乙酰唑胺。这两种药物都能持续刺激呼吸中枢,降低Eupneic PCO 2从而减少植物的生长,增加二氧化碳储备如图7所示。这种相对简单的预防铅和CHF中的血气干扰问题值得进一步研究。不同的患者群体。短效镇静剂,如苯二氮卓三唑仑也被用于CSA患者。理论上,这些药物可以通过抑制呼吸来稳定呼吸。唤醒和巩固睡眠。然而,这种治疗在改善呼吸稳定性方面效果甚微,不推荐。
考虑到铅的机制因患者而异,因此上述疗法可能需要重新评估,并应用于选择性治疗。根据患者的病理生理特征。对那些不愿意接受治疗的人的替代疗法对现有的治疗方法作出反应,需要根据指定这些患者的特征/表型。
总之,睡眠相关的铅很容易被诊断出来,但很难治疗。铅的多重贡献者阻碍了找到有效的治疗方法。未来的研究应该专注于寻找综合治疗的新方法。
总结
pb是一个涵盖许多病理过程的通用术语。这篇评论集中在特定类型的呼吸暂停:非高碳酸的CSA,睡眠诱导呼吸控制的表现不稳定。中枢性睡眠呼吸暂停不是单一疾病,而是呼吸控制系统的紊乱。由多种因素相互作用引起的。睡眠相关因素包括行为控制的觉醒、刺激、静默和动态变化睡眠阶段和从睡眠中唤醒。心血管因素包括心力衰竭相关随着CBF的降低和肺楔压的增加,血流动力学改变以及夜班。除了这些间接原因外,呼吸控制系统被强调:外周和外周的作用和相互作用。铅形成过程中的中心化学受体;CO 2的重要性在维护中呼吸节律性;呼吸驱动功能与无人机之间的恶性循环障碍物。尽管所有的CSA都没有相同的原因,但由于PACO 2的突然和短暂降低,导致呼吸驱动力的停止。呼吸暂停阈值以下是常见的最终路径。小二氧化碳储备、高循环增益和高r-uaw使个人倾向于睡眠时呼吸不稳定和中枢性呼吸暂停。由于相关的复发性缺氧、呼吸急促,铅对健康有显著影响。交感神经活动、重复性觉醒和睡眠碎片。当铅在疾病中出现时,例如与CHF相关,可能对临床结果产生负面影响。近年来,人们在了解铅的病理生理学方面取得了相当大的进展。今后的工作应该继续阐明每种类型的呼吸暂停,目的是将当前的知识转化为临床实践并改进治疗。
相关推荐:



